Chemie der Silane
2. Die Hydrochlorierung von Silicium
Als Hydrochlorierung wird die Umsetzung von Silicium mit Chlorwasserstoff zu Trichlorsilan bezeichnet (Gl. 2).

Allerdings stellt Gl. 2 nur eine Vereinfachung dar, da als Nebenprodukte Siliciumtetrachlorid, Dichlorsilan sowie eine Vielzahl weitere Verbindungen, wie z.B. BCl3, B2H6, AsCl3, PCl3 oder POCl3 entstehen, die vor der weiteren Verwendung des Trichlorsilans in mehreren Reinigungsschritten destillativ entfernt werden müssen. Nach der Trennung wird hochreines Trichlorsilan erhalten, welches die Basis zur Gewinnung von Reinstsilicium für die Halbleiter- und Solarsiliciumproduktion bildet.
Eine treffendere Beschreibung der Hydrochlorierung wird durch (Gl. 3) gegeben.
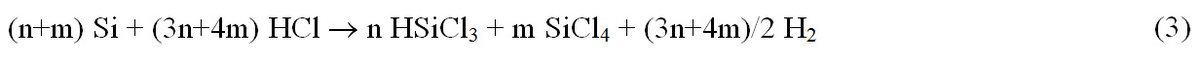
Die allgemeinen Erfahrungen besagen, dass (a) die Reaktion bei umso niedrigerer Temperatur einsetzt, je höher der Metallgehalt des verwendeten Siliciums ist und (b) die Selektivität der Reaktion bezüglich Trichlorsilan umso höher ist, je niedriger der Metallgehalt des Siliciums und je niedriger die Reaktionstemperatur ist. Diese zwei empirisch gefundenen Abhängigkeiten variieren in ihrem Ausmaß mit dem anwesenden Metall und dessen Gehalt im Silicium und zeigen für verschiedene Metalle zudem voneinander abweichende Temperaturabhängigkeiten.
Die anwesenden Metalle und die gewählte Reaktionstemperatur beeinflussen auch die Bildung der Nebenprodukte Siliciumtetrachlorid und Dichlorsilan. Je nach Wahl der Reaktionstemperatur und des Metallgehaltes im Silicium kann der Anteil an Dichlorsilan zwischen 0 und 18 % und der von Siliciumtetrachlorid 0 bis 30 % erreichen [2]. Andererseits können nur in Anwesenheit von Metallen eine hinreichende Reaktionsgeschwindigkeit und hinreichend niedrige Reaktionstemperaturen erzielt werden. Detaillierte Untersuchungen in der Arbeitsgruppe von Prof. H.A. Øye, Universität Trondheim, zeigten, dass die im Silicium enthaltenen intermetallischen Phasen die eigentlichen Reaktionszentren darstellen, die je nach Zusammensetzung jedoch ein unterschiedliches Reaktionsverhalten zeigen [3, 4]. Kinetische und thermodynamische Betrachtungen zur Reaktivität der silicidischen Phasen waren Gegenstand zahlreicher Untersuchungen [5-7].
