Chemie der Silane
1. Die Direkte Synthese oder die Müller-Rochow-Reaktion
Die als Direkte Synthese oder auch als Müller-Rochow-Reaktion benannte Umsetzung von Silicium mit Methylchlorid (Gl. 1) kann als der wichtigste großtechnische Prozess der industriellen Siliciumchemie bezeichnet werden.

Hierbei wird gasförmiges Monochlormethan (Methylchlorid) bei Temperaturen um ca. 300 °C mit Silicium zur Reaktion gebracht, dem Kupfer und weitere Metallverbindungen zugesetzt wurden. Neben dem Zielprodukt Dimethyldichlorsilan entstehen Methyltrichlorsilan und Trimethylchlorsilan sowie eine Reihe niedrigsiedender Verbindungen.

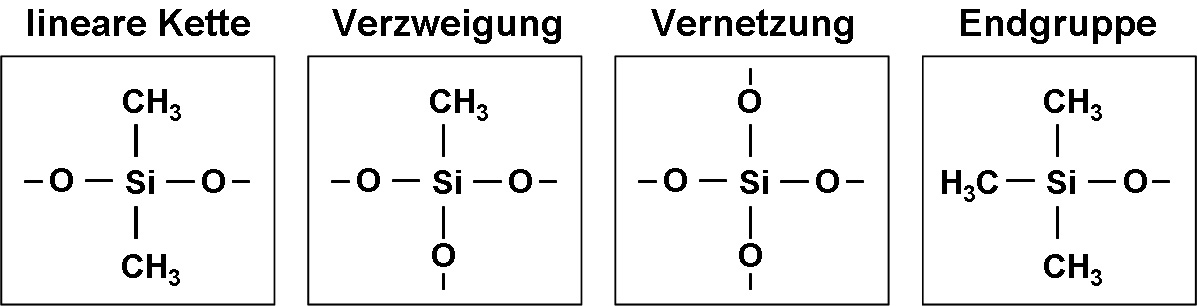
Ausgehend von den Methylchlorsilanen können - ähnlich einem Baukastenprinzip - Grundbausteine für den Aufbau von polymeren Siliconverbindungen mit teilweise komplexen dreidimensionalen Strukturen hergestellt werden (Abb. 2).
Die Direkte Synthese führt nur dann zu den gewünschten Produkten in hohen Raum-Zeit-Ausbeuten, wenn neben dem vorgelegten Silicium bestimmte Metalle anwesend sind. Im industriellen Maßstab werden die erforderlichen Metallgehalte durch Zugabe von Kupfer bzw. Kupferverbindungen zum Silicium, der sogenannten Kontaktmasse, gewährleistet. Hierin liegt das grundlegende Prinzip aller direkten Reaktionen von Silicium (hierunter zählt auch die Umsetzung von Silicium mit Chlorwasserstoff oder mit Alkoholen): Die Steuerung der Reaktivität des eingesetzten Siliciums durch Metalle.
Die Gegenwart von Metallen beeinflusst sowohl die Reaktionstemperatur wie auch die Produktverteilung und die Ausbeute in entscheidendem Maße. So wird das industriell bedeutsame Dimethyldichlorsilan, das in Abwesenheit von Metallen nicht gebildet wird, nur in Anwesenheit von Kupfer und meist zusätzlich unter Einsatz geeigneter Promotoren wie Zink oder Zinn in Ausbeuten zwischen 75 % und 95 % erhalten.
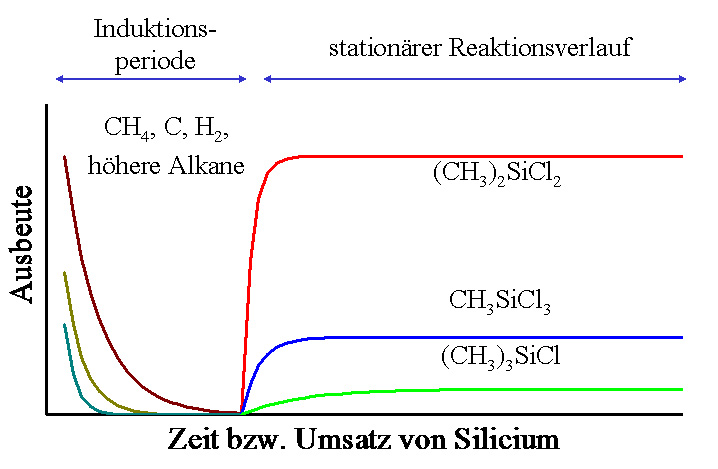
Ein weiteres interessantes Merkmal der Direkten Reaktionen ist eine mehr oder weniger stark ausgeprägte Induktionsperiode (Abb. 3), in der die entstehenden gasförmigen Reaktionsprodukte in ihrer Art und ihrem Anteil sehr unterschiedlich von der Produktverteilung in der stationären Periode der Reaktion ausfallen können. Das Auftreten einer Induktionsperiode, ihre Dauer und die darin auftretende Produktverteilung hängen von den zugegebenen Metallen und deren Zustand ab. Letzterer wird wiederum von den Reaktionsbedingungen während der Induktionsperiode und zusätzlich von den häufig durchgeführten Aktivierungsschritten vor der eigentlichen Umsetzung bestimmt.
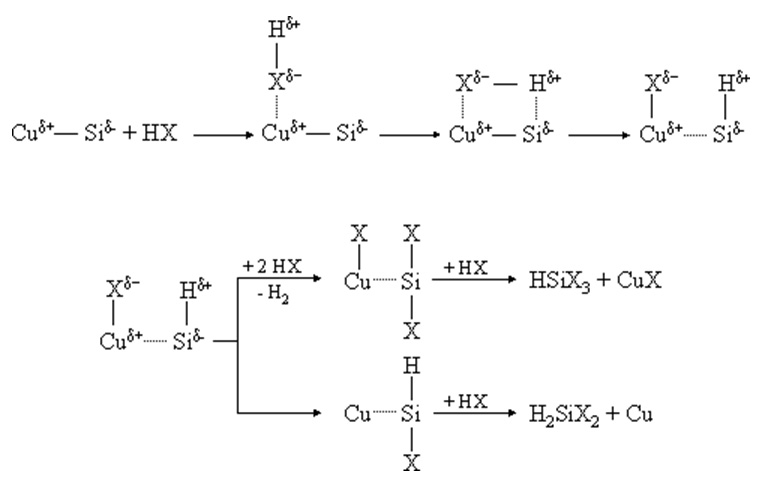
Der Mechanismus der Direkten Synthese ist bis heute nicht vollständig verstanden. Die umfassendste und heute allgemein akzeptierte Interpretation geht auf die Arbeiten von K. M. Lewis zurück. Aufbauend auf dem massenspektroskopischen Nachweis des Methylchlorsilylens (CH3SiCl) formulierten Lewis et al. [1] erstmals einen Silylenmechanismus zur Direkten Synthese (Abb. 4).
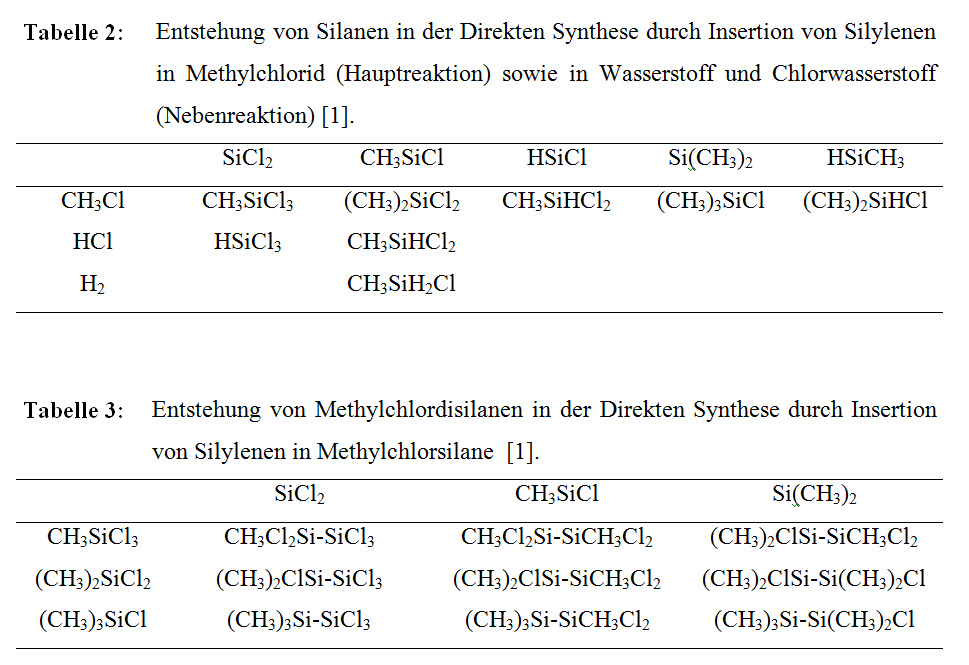
Dieses Modell beschreibt den Reaktionsverlauf als Insertion oberflächlich gebundener Silylene in adsorbierte Eduktmoleküle. Dabei wird vorausgesetzt, dass die Silylene durch ein Substrat, d.h. durch die Kontaktmasse oder den Katalysator, entsprechend stabilisiert werden. Diesem Mechanismus zufolge werden alle primären Hauptprodukte durch Insertion der Silylene CH3SiCl, SiCl2, Si(CH3)2, HSiCl und CH3SiH in die C-Cl-Bindung von adsorbiertem Methylchlorid gebildet (Tab. 2). Disilane entstehen durch Insertion der Silylene in die primär entstandenen Silane (Tab. 3).
Nach Lewis et al. führt die Gegenwart von Kupfer führt zur Bildung von Cu-Si-Bindungen, die durch Elektronenübergang vom Kupfer auf Silicium und eine Rückbindung von Si(3p) auf Cu(3d) gebildet wird, wodurch die Rückbindung der Siliciumoberflächenatome zur Volumenphase geschwächt wird. Liegen infolge der Chemisorption von Methylchlorid CH3SiCl-Silylene vor, tritt das Elektronenpaar des Singulett-Silylens CH3SiCl in Wechselwirkung mit dem teilweise gefüllten 4s-Orbitals des Kupfers, wobei ein freies p-Orbital am Si verbleibt. Dieses freie elektrophile Orbital des Silylens weist in Richtung der Gasphase, wo es zur Insertion in ein adsorbiertes Methylchloridmolekül bereitsteht.
weiter mit...
- 2. Die Hydrochlorierung von Silicium
- 3. Siliciumtetrachlorid - Nebenprodukte der Siliciumabscheidung
- 4. Die homogenphasige Konvertierung von Siliciumterachlorid zu Trichlorsilan
- 5. Die Hydrodechlorierung von SiCl4 in Gegenwart von Silicium
- 6. Die silicidphasenkatalysierte Hydrodechlorierung von Siliciumtetrachlorid
